Azobenzeno
| Azobenzeno Alerta sobre risco à saúde | |
|---|---|
| |
| |
| Nome IUPAC | (E)-diphenyldiazene |
| Outros nomes | Azobenzeno |
| Identificadores | |
| Número CAS | |
| Número RTECS | CN1400000 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | C12H10N2 |
| Massa molar | 182.22 g/mol |
| Aparência | cristais laranja avermelhados |
| Densidade | 1.09 g/cm³, sólido |
| Ponto de fusão |
69 °C (342 K) |
| Ponto de ebulição |
293 °C (566 K) |
| Solubilidade em água | 2.4e-6 g/100mL (25 °C) |
| Acidez (pKa) | 3.3 |
| Estrutura | |
| Forma molecular | sp² at N |
| Momento dipolar | 0 D (trans isomer) |
| Riscos associados | |
| Principais riscos associados |
tóxico |
| Frases R | 45-20/22-48/22-50/53-68 |
| Frases S | 53-45-60-61 |
| Ponto de fulgor | 476 °C |
| Compostos relacionados | |
| Azo-compostos relacionados | Amarelo de anilina (Para-amino-azobenzeno) 4-Hidroxifenilazobenzeno Amarelo de metilo (4-Dimetilaminoazobenzeno) |
| Compostos relacionados | Nitrosobenzeno Anilina |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
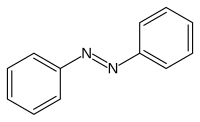
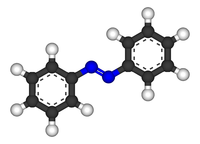
Azobenzeno ou difenildiazeno é um composto químico formado de dois anéis fenila ligados por uma ligação dupla N=N. O termo 'azobenzeno' ou simplesmente 'azo' é frequentemente usado para referir-se a uma grande classe de moléculas que compartilham o centro estrutural azobenzeno, com diferentes grupos funcionais estendidos dos anéis fenila. Estes compostos são formalmente tratados como 'diazenos'. Os diazenos absorvem fortemente luz e são historicamente usados como corante em uma variedade de indústrias.
Síntese
editarAzobenzeno foi primeiro descrito em 1856 como "gelblich-rothe krystallinische Blättchen" (lâminas cristalinas amareladas).[1] A preparação original é similar à moderna. De acordo com o método de 1858, nitrobenzeno é reduzido por limalha de ferro na presença de ácido acético. Na síntese moderna, zinco é o redutor na presença de uma base, como descrito por Bigelow e Robinson,[2][3] em modificação do método original de Alexejew.[4]
O azobenzeno tem sido preparado por muitas maneiras diferentes, das quais as seguintes são representativas: pode ser obtido por redução de nitrobenzeno amálgama de sódio,[5] com sulfetos alcalinos,[6] com celulose,[7] molasses[8] ou dextrose[8] em solução alcalina, e por redução catalítica.[9]
O azobenzeno também pode ser obtido da redução de anilina diazotada com sais de cobre (I) (sais cuprosos).[10]
Anilina tem sido oxidada, resultando em azobenzeno, por ar[11] e por permanganato de potássio.[12]
A condensação de nitrobenzeno e acetato de anilina também rende como produto azobenzeno.[13]
Isomerização trans-cis
editarUma das mais intrigantes propriedades do azobenzeno (e derivados) é a fotoisomerização dos isômero trans e cis. Os dois isômeros podem passar de um para outro com particulares comprimentos de onda de luz: luz ultravioleta, as quais corespondem a energia do lacuna da transição π-π* (estado S2), para conversão trans-a-cis, e luz azul, a qual é equivalente a transição n-π* (estado S1), para isomerização cis-a-trans. Por uma variedade de razões, o isômero cis é menos estável que o trans (por exemplo, tem uma configuração distorcida e é menos acomodado - mais "tenso" - do que a configuração trans). Então, o cis-azobenzeno irá termicamente relaxar novamente ao trans via isomerização cis-a-trans. O isômero trans é mais estável em aproximadamente 50 kJ/mol, e a barreira à foto-isomerização é aproximadamente 200 kJ/mol.
Classificação espectroscópica
editarOs comprimentos de onda nas quais a isomerização do azobenzeno ocorre depende da estrutura particular de cada molécula de composto azo, mas elas são tipicamente agrupadas em três classes: as moléculas do tipo azobenzeno, os aminoazobenzenos, e os pseudo-estilbenos.[14] Estes compostos azos são amarelos, alarnjados e vermelhos, respectivamente,[15] devido às diferenças sutis em seus espectros de absorção eletrônica. Os compostos similares aos compostos azobenzeno não substituídos exibem uma baixa densidade de absorção n-π* na região do visível, e uma muito mais alta densidade de absorção π-π* na região do ultravioleta. Composto azo que são orto- ou para-substituídos com grupos doadores de elétrons (tais como aminos), são classificados como aminoazobenzenos, e tendem a apresentar pequeno espaçamento[14] nas bandas n-π* e π-π* no visível. A classe pseudo-estilbeno é caracterizada pela substituição das posições 4 e 4' dos dois anéis azo com doadores de elétrons e elétrons que retiram dos grupos (isto é, as duas extremidades opostas do sistema aromático são funcionalizadas). A adição desta configuração "push-pull" resulta em uma distribuição eletrônica fortemente assimétrica, a qual modifica uma série de propriedades ópticas. Em particular, ela desloca o espectro de absorção dos isômeros trans e cis, de modo que eles se sobrepõem de forma eficaz.[15] Assim, para estes compostos um único comprimento de onda de luz na região visível irá induzir isomerização tanto para a frente como reversa. Sob iluminação, estas moléculas ficam em ciclo entre os dois estados isoméricos.
Fotofísica da isomerização
editarA fotoisomerização do azobenzeno é extremamente rápida, ocorrendo na escala de picosegundos. A taxa do relaxamento de retorno térmico varia grandemente dependendo do composto: usualmente horas para as moléculas do tipo do azobenzeno, minutos para aminoazobenzenos, e segundos para os pseudo-estilbenos.[15]
O mecanismo de isomerização tem sido objeto de algum debate, com dois caminhos identificados como viáveis: uma rotação sobre a ligação N-N, com ruptura da ligação dupla, ou via uma inversão, com um estado de transição hibridizado e semilinear. Tem sido sugerido que a conversão de trans-para-cis ocorre via rotação no estado S2, enquanto a inversão ocorre na conversão cis-para-trans. Está ainda em discussão qual estado excitado desempenha um papel direto na série do comportamento de fotoisomerização. Entretanto, as mais recentes pesquisas em espectroscopia de transição de femtosegundo tem sugeridos que o estado S2 sofre conversão interna ao estado S1, e então a isomerização trans-para-cis ocorre. Recentemente, um outro caminho de isomerização foi proposto por Diau,[16] a via da "inversão concertada" em que ambos os ângulos de ligação CNN curvam-se ao mesmo tempo.
Movimentos fotoinduzidos
editarA fotoisomerização do azobenzeno é uma forma de movimento molecular fotoinduzido.[14][17][18] Esta isomerização pode também conduzir a movimento em maiores escalas de comprimento. Por exemplo, luz polarizada fará com que as moléculas isomerizem-se e relaxem em posições aleatórias. No entanto, aquelas moléculas (trans) relaxadas que situam-se perpendicularmente à polarização da luz incidente deixarão de ser capazes de absorver, e irão permanecer imutáveis. Assim, existe um enriquecimento na estatística dos cromóforos perpendiculares à luz polarizada (revelação de furo orientacional). A irradiação polarizada fará um material azo anisotrópico e, portanto, opticamente birrefringente e dicróico. Esta foto-orientação pode também ser utilizada para orientar outros materiais (especialmente nos sistemas de cristal líquido).[19] Por exemplo, tem sido utilizada para orientar seletivamente domínios de cristal líquido, e para criar materiais de ópticas não lineares (NLO, do inglês nonlinear optical). Isomerização azo também pode ser usada para foto-alternar a fase de cristal líquido de um material de colestérico a nemático[20][21] ou para mudar o campo de uma fase colestérica.[22]
Em 1995, foi relatado que expondo-se uma película fina de azo-polímero a um gradiente de intensidade (ou polarização) de luz conduz a padrões espontâneos de superfície. Em essência, o material polímero irá deformar-se reversivelmente de maneira a minimizar a quantidade de material exposto à luz. Este fenômeno não é ablação por laser, dado que facilmente ocorre a baixa potência e a transformação é reversível. O mecanismo desta holografia de superfície parece estar associado a um novo efeito fotomecânico, envolvendo a isomerização do azobenzeno.[23]
Expansão e contração em maiores escalas de materiais azobenzênicos também foram observadas. Num relatório, uma película fina foi feita para dobrar-se e afrouxar-se expondo-a à luz polarizada. A direção do movimento no macroscópico poderia ser controlado pela direção da polarização. A flexão ocorre porque a superfície livre do material contrai-se mais do que o interior da película fina (devido à absorção de luz laser que passa através da película).
Outros aspectos
editarMoléculas de azobenzeno podem ser incorporadas em matrizes de polímeros como estabilizadores. é também interessante se notar que a estrutura rígida como uma barra de moléculas azo lhes permite comportar-se como mesogens de cristal líquido em muitos materiais.
A modificação da geometria em maior escala associada com a fotoisomerização do azobenzeno também tem sido utilizada para controlar a atividade de proteínas com a luz. Ao azobenzeno tem sido atribuída a ligantes (drogas) para fotomodular a sua afinidade para as proteínas. Azobenzeno tem sido empregado como um tirante fotointercambiável entre um ligante e a proteína: uma extremidade do azobenzeno é substituída com um grupo reativo que se liga à proteína alvo. A outra extremidade apresenta um ligante para a proteína. Dependendo do local onde o azobenzeno está acoplado, enquanto o isômero trans ou cis apresenta o ligante para o local de ligação, o outro isômero impede que o fármaco aproxime-se do local. Mais uma vez, o fotointercâmbio entre isômeros transforma a proteína ligando-se e desligando-se. Quando aplicado a canais iônicos no sistema nervoso, esta abordagem proporciona controle óptico de atividade elétrica nos neurônios.[24][25]
Referências
- ↑ Noble, A. "Zur Geschichte des Azobenzols und des Benzidins" Annalen der Chemie und Pharmacie 1856, Volume 98, p 253-256. doi:10.1002/jlac.18560980211 .
- ↑ Bigelow, H. E.; Robinson, D. B. "Azobenzene" Organic Syntheses, Collected Volume 3, p.103 (1955). http://www.orgsyn.org/orgsyn/pdfs/CV3P0103.pdf
- ↑ Nobel, Ann., 98, 253 (1856).
- ↑ Alexejew, Z. Chem., 4, 497 (1868).
- ↑ Werigo, Ann., 135, 176 (1865).
- ↑ Lucius and Bruning, Ger. pat. 216,246 [C. A., 4, 813 (1910)].
- ↑ Greisheim, Ger. pat. 225,245 [C. A., 5, 592 (1911)].
- ↑ a b Opolonick, Ind. Eng. Chem., 27, 1045 (1935).
- ↑ Treed and Signaigo, U. S. pat. 2,344,244 [C. A., 38, 3663 (1944)]; Henke and Brown, J. Phys. Chem., 26, 324, 631 (1922).
- ↑ Bozoslavski, J. Gen. Chem. U.S.S.R., 16, 193 (1946).
- ↑ Alekseevskii and Golbrakht, Russ. pat. 32,499 [C. A., 28, 3425 (1934)]; Brown and Triske, J. Phys. & Colloid Chem., 51, 1394 (1947).
- ↑ Glaser, Ann., 142, 364 (1867).
- ↑ Baeyer, Ber., 7, 1638 (1874).
- ↑ a b c H. Rau, in Photochemistry and Photophysics; Vol. 2, edited by J. Rebek (CRC Press, Boca Raton, FL, 1990), p. 119-141.
- ↑ a b c Intelligent Materials [Online]; Shahinpoor, M.; Schneider, H.-J. Eds.; Royal Society of Chemistry:Cambridge, 2008; p 426–427. http://books.google.lv/books?id=Hmq4ctnA1KIC&pg=PA426&lpg=PA426&dq=pseudo+stilbene&source=bl&ots=zV6JZtmLEa&sig=de7ZDSJG2LkSBupqZgBle4n-7j8&hl=ru&sa=X&ei=Y-z8TrjAJoLj4QT93MmNCA&redir_esc=y#v=onepage&q=pseudo%20stilbene&f=false (accessed Dec 30, 2011).
- ↑ Wei-Guang Diau, Eric (2004). «A New Trans-to-Cis Photoisomerization Mechanism of Azobenzene on the S1(n,π*) Surface». The Journal of Physical Chemistry A. 108 (6). 950 páginas. doi:10.1021/jp031149a
- ↑ Natansohn A, Rochon P. «Photoinduced motions in azo-containing polymers». Chem. Rev. 102 (11): 4139–75. PMID 12428986
- ↑ Yu, Yanlei; Nakano, Makoto; Ikeda, Tomiki (2003). «Photomechanics: Directed bending of a polymer film by light». Nature. 425 (6954). 145 páginas. PMID 12968169. doi:10.1038/425145a
- ↑ Ichimura, Kunihiro (2000). «Photoalignment of Liquid-Crystal Systems». Chemical Reviews. 100 (5): 1847–1874. PMID 11777423. doi:10.1021/cr980079e
- ↑ Tazuke, Shigeo; Kurihara, Seiji; Ikeda, Tomiki (1987). «Amplified image recording in liquid crystal media by means of photochemically triggered phase transition». Chemistry Letters (5). 911 páginas. doi:10.1246/cl.1987.911
- ↑ Tamaoki, N. (2001). «Cholesteric Liquid Crystals for Color Information Technology». Advanced Materials. 13 (15). 1135 páginas. doi:10.1002/1521-4095(200108)13:15<1135::AID-ADMA1135>3.0.CO;2-S
- ↑ Pieraccini, Silvia; Masiero, Stefano; Spada, Gian Piero; Gottarelli, Giovanni (2003). «A new axially-chiral photochemical switch». Chemical Communications (5). 598 páginas. doi:10.1039/b211421f
- ↑ Kevin G. Yager and Christopher J. Barrett (2006). «Photomechanical Surface Patterning in Azo-Polymer Materials». Macromolecules. 39 (26): 9320–6. doi:10.1021/ma061733s
- ↑ Gorostiza, P.; Isacoff, E. Y. «Optical switches for remote and noninvasive control of cell signaling». Science. 322 (5900): 395–399. PMID 18927384. doi:10.1126/science.1166022
- ↑ Banghart, M. R.; Volgraf, M.; Trauner, D. «Engineering light-gated ion channels». Biochemistry. 45 (51): 15129–15141. PMID 17176035. doi:10.1021/bi0618058
Leitura adicional
editar- H. Rau, in Photochemistry and Photophysics; Vol. 2, edited by J. Rebek (CRC Press, Boca Raton, FL, 1990), p. 119-141.
- A. Natansohn and P. Rochon, Chem. Rev. 102, 4139-4176 (2002).
- Y. Yu, M. Nakano, and T. Ikeda, Nature (London, U. K.) 425, 145 (2003).