Tacrolimo
| Tacrolimo Alerta sobre risco à saúde | |
|---|---|
| |
| |
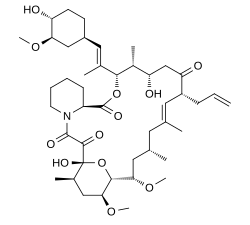
| Nome IUPAC | (−)-(3S,4R,5S,8R,9E,12S,14S,15R,16S,18R,26aS)-8-allyl-5,6,8,11,12,13,14,15,16,17,18,19,24,25,26,26a-hexadecahydro-5,19-dihydroxy-3-{(E)-2-[(1R,3R,4R)-4-hydroxy-3-methylcyclohexyl]-1-methylvinyl}-14,16-dimethoxy-4,10,12,18-tetramethyl-15,19-epoxy-3H-pyrido[2,1-c][1,4]oxaazacyclotricosane-1,7,20,21(4H,23H)-tetrone |
| Identificadores | |
| Número CAS | |
| PubChem | |
| DrugBank | DB00864 |
| KEGG | |
| ChEBI | |
| Código ATC | D11 |
| SMILES |
|
| DCB n° | 09719 |
| Primeiro nome comercial ou de referência | Prograf, Advagraf, Protopic |
| Propriedades | |
| Fórmula química | C44H69NO12 |
| Massa molar | 803.95 g mol-1 |
| Farmacologia | |
| Biodisponibilidade | 24% (5–67%), menor após alimento gorduroso |
| Via(s) de administração | Tópico, oral, intravenoso |
| Metabolismo | Liver CYP3A4, CYP3A5 |
| Ligação plasmática | ≥98.8% |
| Excreção | Mostly fecal |
| Classificação legal |
℞-only (US) |
| Riscos na gravidez e lactação |
C(AU) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Tacrolimo (também conhecido como FK-506 ou fujimicina) é um fármaco imunossupressor da classe dos inibidores de calcineurina, usado principalmente após transplante de órgão para reduzir a atividade do sistema imune e, assim, reduzir o risco de rejeição. Atua reduzindo a atividade de linfócitos T e a interleucina 2 (IL-2).[1]

Usos
editarÉ usado especialmente para evitar a rejeição de órgãos transplantados, mas também pode ser usado na preparação da pele para o tratamento de dermatite atópica, uveíte e vitiligo com 4 anos ou mais.[2]
Embora o efeito imunossupressor e sobrevivência de curto prazo foi demonstrado ser semelhante a da ciclosporina, os resultados com tacrolimo tiveram um perfil lipídico mais favorável, e isso tem importantes implicações a longo prazo sobre o prognóstico, dada a influência a longo prazo sobre a rejeição e sobrevida do enxerto.[3]
Farmacocinética
editarQuando administrado oralmente, seu metabolismo é hepático (CYP3A4) com meia-vida de 11,3 h, em média (gama 3,5-40,6 h) e sua excreção é na maioria fecal. Sua biodisponibilidade é de 20%, sendo menor depois de comidas gordurosas.
Efeitos adversos
editarSeus efeito adverso mais comuns incluem sensação de queimação na pele, prurido, dermatite, vermelhidão e sintomas de gripe como náusea e dor de cabeça.[4]
O uso de tacrolimus tópico deve ser evitado em caso de suspeita de lesões malignas, nem deve ser associado a bandagens oclusivas. Como é um imunosupressor, diminui a resposta do organismo a infecções e neoplasias.[5]
Contraindicações
editarÉ contraindicada em caso de gravidez, lactância, infecções, neoplasias, problemas hepáticos. Recomenda-se evitar a luz solar direta e o consumo de toranja (grapefruit) após seu uso.[6]
História
editarFoi descoberto por uma equipe japonesa em 1984 a partir do caldo de fermentação de uma amostra de solo contendo a bactéria Streptomyces tsukubaensis japonesa. Foi aprovado pela FDA para uso humano em 1994.[7]
Referências
- ↑ J.G. O'Grady, A. Burroughs, P. Hardy, D. Elbourne, A. Truesdale, and The UK and Ireland Liver Transplant Study Group (2002). «Tacrolimus versus emulsified cyclosporin in liver transplantation: the TMC randomised controlled trial.». Lancet 360: pp. 1119–1125. doi:10.1016/S0140-6736(02)11196-2.
- ↑ Hanifin, Jon M.; Paller, Amy S.; Eichenfield, Lawrence; Clark, Richard A.; Korman, Neil; Weinstein, Gerald; Caro, Ivor; Jaracz, Eileen; Rico, M. Joyce (1 de agosto de 2005). «Efficacy and safety of tacrolimus ointment treatment for up to 4 years in patients with atopic dermatitis». Journal of the American Academy of Dermatology (em inglês) (2): S186–S194. ISSN 0190-9622. doi:10.1016/j.jaad.2005.04.062. Consultado em 11 de janeiro de 2021
- ↑ M.M. Abou-Jaoude, R. Naim, J. Shaheen, N. Naufal, S. Abboud, M. AlHabash, M. Darwish, A. Mulhem, A. Ojjeh, and W.Y. Almawi (2005). «Tacrolimus (FK506) versus cyclosporin microemulsion (Neoral) as maintenance immunosuppresion therapy in kidney transplant recipients.». Transplantation Proceedings 37: pp. 3025–3028. doi:10.1016/j.transproceed.2005.08.040.
- ↑ «Tacrolimus: MedlinePlus». medlineplus.gov (em espanhol). Consultado em 11 de janeiro de 2021
- ↑ «Protopic (Tacrolimus): Uses, Dosage, Side Effects, Interactions, Warning». RxList (em inglês). Consultado em 11 de janeiro de 2021
- ↑ Fukatsu S, Fukudo M, Masuda S, Yano I, Katsura T, Ogura Y, Oike F, Takada Y, Inui K (2006). «Delayed effect of grapefruit juice on pharmacokinetics and pharmacodynamics of tacrolimus in a living-donor liver transplant recipient». Drug Metab Pharmacokinet 21 (2): pp. 122–5. doi:10.2133/dmpk.21.122. PMID 16702731.
- ↑ Kino T, Hatanaka H, Hashimoto M, Nishiyama M, Goto T, Okuhara M, Kohsaka M, Aoki H, Imanaka H (1987). «FK-506, a novel immunosuppressant isolated from a Streptomyces. I. Fermentation, isolation, and physico-chemical and biological characteristics.». J Antibiot (Tokyo) 40 (9): pp. 1249–55. PMID 2445721.