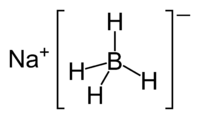
Borohidreto de sódio
Borohidreto de sódio,[2] também conhecido como tetraidroborato de sódio, tem fórmula química NaBH4. Esse sólido branco, usualmente encontrado como um pó, é um agente redutor especialmente usado na produção de fármacos e outros compostos orgânicos e inorgânicos. É solúvel em metanol e água, mas reage com ambos na ausência de uma base.[3]
O composto foi descoberto nos anos 1940 por H. I. Schlessinger, que conduziu uma equipe que desenvolveu borohidretos de metais para aplicações em tempo de guerra.[4]
Síntese e manuseio
editarborohidreto de sódio é preparado pela reação de hidreto de sódio sobre borato de trimetila a 250-270 °C:
- B(OCH3)3 + 4 NaH → NaBH4 + 3 NaOCH3
Ele pode também ser produzido pela reação de NaH sobre vidro borossilicato pulverizado.[5]
NaBH4 pode ser recristalizado por dissolução em diglima morna (50 °C) seguido pelo esfriamento da solução.[6]
Reatividade
editarAplicações em síntese orgânica
editarborohidreto de sódio reduz aldeídos e cetonas em álcoois, assim como os mais reativos derivados de ácidos carboxílicos, cloretos de acila e ésteres de tiol. Entretanto, diferentemente do poderoso agente redutor hidreto de lítio e alumínio, o uso único de NaBH4 com condições de reação mais suaves não irá reduzir ésteres, amidas, ou ácidos carboxílicos.[3] Um exemplo do uso do borohidreto de sódio é a produção industrial de fexofenadina a qual inclui como passo uma redução:[7]
Reagentes relacionados
editarA atividade de agentes redutores de borohidreto podem ser atenuadas por estabilização da ligação boro-hidreto. Isto é feito através da ligação de grupos volumosos estericamente ou grupos que façam a remoção de elétrons. Grupos acetil (triacetoxiborohidreto de sódio, (NaBH(OCOCH3)3) ou ciano (cianoborohidreto de sódio (NaCNBH3)) têm sido usados com este propósito. Como resultado, procuram-se uso na reação de aminação redutiva. Aqui, o intermediário imina pode ser seletivamente reduzido na presença do material de partida aldeído ou cetona.
Agentes redutores mais fortes podem ser gerados por desestabilização da ligação boro-hidreto. Isto é encontrado em compostos tais como superidreto (trietilborohidreto de lítio) e L-Selectrida (tri-sec-butilborohidreto de lítio).[8]
Outras reações
editarOxidação de NaBH4 com iodo em tetraidrofurano cria o complexo BH3-THF, o qual pode reduzir ésteres. O mesmo modo o sistema NaBH4-MeOH, formado pela adição de metanol a borohidreto de sódio em THF em refluxo reduz ésteres aos álcoois correspondentes como por exemplo o benzoato de benzila a álcool benzílico.[9]
Células combustível
editarborohidreto de sódio é também usado em sistemas de células combustível experimentais. Como combustível é menos inflamável e menos volátil que gasolina mas mais corrosivo. É relativamente pouco agressivo ambientalmente devido a baixa toxidade dos boratos. O hidrogênio é gerado para um célula combustível por decomposição catalítica da solução aquosa de borohidreto:
- NaBH4 + 2 H2O → NaBO2 + 4 H2
Referências
- ↑ a b MSDS data (carl roth)
- ↑ «RUN: Montagem e caracterização de uma pilha de combustível de borohidreto / peróxido de hidrogénio». doi:10362/6569 Verifique
|doi=(ajuda) - ↑ a b Banfi, L.; Narisano, E.; Riva, R. “Sodium Borohydride” in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York,doi:10.1002/047084289X.rs052.
- ↑ Schlesinger, H. I.; Brown, H. C.; Abraham, B.; Bond, A. C.; Davidson, N.; Finholt, A. E.; Gilbreath, J. R.; Hoekstra, H.; Horvitz, L.; Hyde, E. K.; Katz, J. J.; Knight, J.; Lad, R. A.; Mayfield, D. L.; Rapp, L.; Ritter, D. M.; Schwartz, A. M.; Sheft, I.; Tuck, L. D.; Walker, A. O. “New developments in the chemistry of diborane and the borohydrides. General summary” Journal of the American Chemical Society 1953, volume 75, pages 186-90,doi:10.1021/ja01097a049.
- ↑ Schubert, F.; Lang, K.; Burger, A. “Alkali metal borohydrides” (Bayer), 1960. German patent DE 1088930 19600915 (ChemAbs: 55:120851). Supplement to . to Ger. 1,067,005 (CA 55, 11778i). From the abstract: “Alkali metal borosilicates are treated with alkali metal hydrides in approx. 1:1 ratio at >100° with or without H pressure”.
- ↑ Brown, H. C. “Organic Syntheses via Boranes” John Wiley & Sons, Inc. New York: 1975. ISBN 0-471-11280-1. page 260-1.
- ↑ SPECIAL FEATURE SECTION: HYDRIDE REDUCTIONS Christian T. Goralski and Bakthan Singaram Org. Process Res. Dev.; 2006; 10(5) pp 947 - 948; (Editorial) doi:10.1021/op0601363
- ↑ Seyden-Penne, J. "Reductions by the Alumino- and Borohydrides in Organic Synthesis"; VCH–Lavoisier: Paris, 1991.
- ↑ da Costa, Jorge C.S.; Karla C. Pais, Elisa L. Fernandes, Pedro S. M. de Oliveira, Jorge S. Mendonça, Marcus V. N. de Souza, Mônica A. Peralta, and Thatyana R.A. Vasconcelos (2006). «Simple reduction of ethyl, isopropyl and benzyl aromatic esters to alcohols using sodium borohydride-methanol system» (PDF). Arkivoc: 128-133. Consultado em 29 de agosto de 2006
11. loucura loucura mesmo