Adamantano
| Adamantano Alerta sobre risco à saúde | |
|---|---|

|
|
| |
| Nome IUPAC | Adamantane[1] |
| Outros nomes | Triciclo[3.3.1.13,7]decano |
| Identificadores | |
| Número CAS | |
| ChemSpider | |
| SMILES |
|
| Propriedades | |
| Fórmula química | C10H16 |
| Massa molar | 136.23 g mol-1 |
| Aparência | Pó branco ou esbranquiçado |
| Densidade | 1.07 g/cm³ (20 °C), sólido |
| Ponto de fusão |
270 °C (543 K) |
| Solubilidade em água | Pouco solúvel |
| Solubilidade em outros solventes | Solúvel em hidrocarbonetos |
| Estrutura | |
| Estrutura cristalina | Sistema cúbico de face centrada |
| Momento dipolar | 0 D |
| Riscos associados | |
| Principais riscos associados |
Inflamável |
| Frases S | 24/25/28/37/45 |
| Compostos relacionados | |
| compostos: relacionados | Memantina Rimantadina Amantadina |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
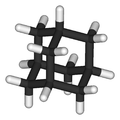
Adamantano (triciclo[3.3.1.13,7]decano) é um composto cristalino incolor, com odor semelhante ao da cânfora.[2] Com fórmula C10H16, é um cicloalcano e também o mais simples dos diamantóides. Foi descoberto no petróleo em 1933.[3] O seu nome deriva do grego adamantinos (relativo ao aço ou diamante), devido à sua estrutura semelhante à do diamante.[4] O adamantano é o isómero mais estável de C10H16.
Síntese
editarO adamantano foi sintetizado pela primeira vez por Vladimir Prelog em 1941.[5][6] Um método mais conveniente foi descoberto por Schleyer em 1957, a partir do diciclopentadieno por hidrogenação seguida de rearranjo por catálise ácida.[7][8]
Usos
editarO adamantano não possui muitas aplicações diretas. É utilizado em algumas máscaras de gravuras secas.[9]
Em espectroscopia de ressonância magnética nuclear de estado sólido, o adamantano é um padrão comum para a referenciação do desvio químico.[10]
Em laseres corantes o adamantano pode ser utilizado para aumentar a vida útil do meio de amplificação; não pode ser fotoionizado sob atmosfera porque as suas faixas de absorção situam-se na região ultravioleta de vácuo do espectro. As energias de fotoionização do adamantano e de outros diamantóides maiores foram determinadas recentemente.[11]
Derivados do adamantano
editarOS derivados do adamantano são úteis em medicina, por exemplo amantadina e rimantadina. Adamantanos condensados ou diamantóides foram isolados a partir de frações de petróleo, onde ocorrem em pequenas quantidades. Estas espécies são de interesse como aproximações moleculares da estrutura cúbica do diamante, terminadas com ligações C-H. O 1,3-deidroadamantano é um membro da família do propelano.
Devido à sua estabilidade, propriedades estéricas específicas e rigidez conformacional, o grupo 1-adamantilo é um substituinte em química orgânica e organometálica. Alguns dos primeiros carbenos persistentes continham substituintes de adamantilo.
Análogos do adamantano
editarMuitas moléculas adotam estruturas em gaiola com estruturas adamantóides. Compostos deste tipo particularmente úteis incluem P4O6, As4O6, P4O10 (= (PO)4O6), P4S10 (= (PS)4S6), e N4(CH2)6.[12]
Referências
- ↑ Segundo a pág. 41 do a 2004 IUPAC guide Arquivado em 17 de dezembro de 2008, no Wayback Machine., adamantano é o "nome IUPAC preferido".
- ↑ «ADAMANTANE(TRICYCLO(3.3.1.1)DECANE)». Consultado em 14 de outubro de 2005. Arquivado do original em 5 de setembro de 2008
- ↑ Landa, S.; Machácek, V. (1933). «Chem. Commun.». Collection Czech. Chem. Commun. 5. 1 páginas
- ↑ Alexander Senning. Elsevier's Dictionary of Chemoetymology. Elsevier, 2006. ISBN 0444522395.
- ↑ Prelog, V., Seiwerth,R. (1941). «Über die Synthese des Adamantans». Berichte. 74: 1644–1648. doi:10.1002/cber.19410741004
- ↑ Prelog, V., Seiwerth,R. (1941). «Über eine neue, ergiebigere Darstellung des Adamantans». Berichte. 74: 1769–1772. doi:10.1002/cber.19410741109
- ↑ Schleyer, P. von R. (1957). «A Simple Preparation of Adamantane». J. Am. Chem. Soc. 79: 3292–3292. doi:10.1021/ja01569a086
- ↑ Schleyer, P. von R.; Donaldson, M. M.; Nicholas, R. D.; Cupas, C. (1973). «Adamantane». Org. Synth.; Coll. Vol., 5
- ↑ Watanabe, Keiji;; et al. (2001). «Resist Composition and Pattern Forming Process». United States Patent Application 20010006752. Bandwidth Market, Ltd. Consultado em 14 de outubro de 2005. Arquivado do original em 4 de setembro de 2011
- ↑ Morcombe, Corey R.; Zilm, Kurt W. (2003). «Chemical Shift referencing in MAS solid state NMR». J. Magn. Reson. 162: 479–486. doi:10.1016/S1090-7807(03)00082-X
- ↑ Lenzke, K. ; Landt, L.; Hoener, M.; et al. (2007). «Experimental determination of the ionization potentials of the first five members of the nanodiamond series». J. Chem. Phys. 127. 084320 páginas. doi:10.1063/1.2773725
- ↑ Vitall, J. J. (1996). «The Chemistry of Inorganic and Organometallic Compounds with Adamantane-Like Structures». Polyhedron. 15: 1585–1642. doi:10.1016/0277-5387(95)00340-1